
Бесплатный фрагмент - Задачи на растворы для экзамена по химии и даже больше
Мой будущий ученик
Возможно, тебе важно спросить:
— «Елена Викторовна, а я точно смогу это понять?»
— Конечно! Мы начнём с самых простых примеров — чай с сахаром, солёная вода, лимонад — и дойдём до таких задач, которые на экзамене принесут баллы легко и без нервов.
Я написала это пособие, потому что слишком часто вижу одну и ту же картину: умные, старательные ребята «спотыкаются» на задачах, которые можно было решить за минуту.
Почему? В школе на тренировки по этой теме почти нет времени. Учебники дают определения, но не учат думать. Интернет полон отдельных объяснений, но они не складываются в целостную картину. В результате теряются баллы на простых вопросах, хотя можно было бы взять максимум.
На самом деле задачи на растворы — это не страшные формулы и проценты, а логика, отточенная до автоматизма. Их можно «прокачать» как навык езды на велосипеде: сначала медленно и неуверенно, потом всё быстрее и точнее.
Здесь мы пойдём пошагово:
▪ {️} разберём все способы выражения состава растворов;
▪ {️} научимся выбирать верную формулу и применять её без долгих колебаний;
▪ {️} отработаем задачи от базового уровня до олимпиадных хитростей.
Многие задачи составлены на примерах из реальной жизни — чтобы ты видел, что химия работает не только в задачниках, но и в твоём стакане с соком, в аптечке и на кухне.
К концу книги ты:
▪ {️} перестанешь путаться в процентах и концентрациях;
▪ {️} будешь решать задачи быстро и уверенно;
▪ {️} получишь прочную базу для более сложных тем химии.
А если хочешь закрепить навык, разобрать личные ошибки и дойти до стабильно высоких баллов на экзамене — присоединяйся к моим занятиям. Там мы доведём этот навык до совершенства.
Готов? Тогда переворачивай страницу — и давай узнаем, что на самом деле скрывает раствор.
Глава 1. Что скрывает раствор
«В растворе, как в отношениях: важно, кто растворяет, а кто — растворяется».
— Кира Дисперсия, блогерша, создатель историй о химии и драме.
Каждый раствор включает два основных компонента:
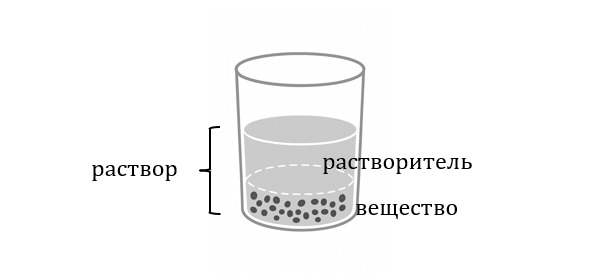
Растворитель — вещество, которого в растворе больше всего. В нём растворяются другие вещества.
Растворяемое вещество — то, что добавляют в растворитель и что в нём растворяется.
Пример: в стакане сладкой воды растворителем будет вода, а растворяемым веществом — сахар.
Важно знать, что растворители и растворяемые вещества могут находиться в разных агрегатных состояниях — твёрдом, жидком или газообразном. Например, в газированных напитках растворён углекислый газ в жидкости, а в воздухе — газы растворены друг в друге.
Учимся считать массы компонентов раствора
Главные формулы:
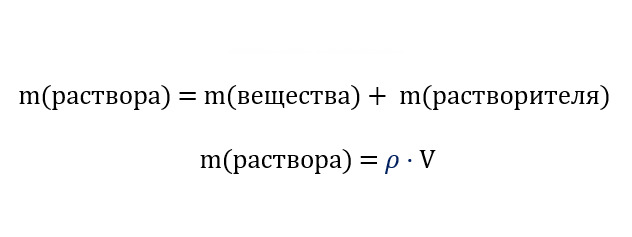
Дополнительные формулы:
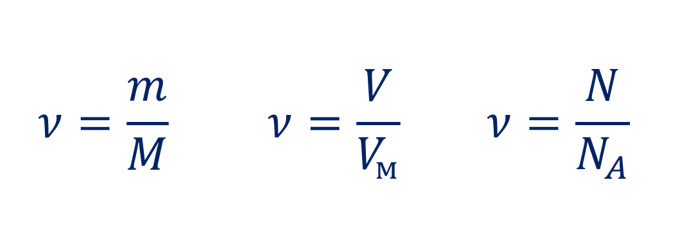
Простые вычисления — домашняя химия
1. Мама собралась солить огурцы. Она растворила 20 г соли в 100 г воды. Какова масса получившегося солёного раствора?
2. Для уборки кухни нужен чистящий раствор. В 1 литре воды растворили 250 г уксуса, 10 г жидкого мыла. Какова масса готового раствора?
3. Чтобы приготовить домашний спортивный напиток, ты растворил в 400 мл воды 10 г сахара, 2 г соли и 30 г апельсинового сока. Сколько граммов напитка получилось?
4. Для 2700 г домашнего лимонада ты взял 350 г сахара и 350 г свежевыжатого лимонного сока. Сколько мл воды ты использовал?
5. Фармацевт собрал по рецепту 700 г лекарственного раствора, растворив в воде 100 г порошка. Сколько граммов воды он использовал?
6. Ты смешал 1000 г медового напитка, в котором содержится 850 г воды и 5 г лимонного сока. Сколько мёда ты добавил в напиток?
7. Ты приготовил 240 г стирального раствора, добавив порошок в воду. В растворе содержится 200 г воды. Сколько порошка ты насыпал?
8. 20 мл аптечного спиртового раствора йода имеют массу 18,4 г. Определи плотность раствора.
9. Во флаконе 150 мл лечебного сиропа от кашля с плотностью 1,1 г/мл. Определи массу этого сиропа.
10. В тюбике 100 мл густого увлажняющего крема. Плотность крема — 1,25 г/мл. Какова его масса?
11. Для подкормки растений был приготовлено 80 мл раствора удобрения с плотностью 1,4 г/мл. Каков по массе этот раствор?
12. Во флаконе с антисептиком содержится 300 г раствора с плотностью 1,2 г/мл. Определи, какой объём занимает раствор антисептика.
13. 7,2 г ванильного экстракта имеют плотность 1,1 г/мл. Сколько миллилитров экстракта ты добавил в тесто?
14. Ты приготовил 84 г раствора жидкого удобрения с плотностью 1,4 г/мл. Определи его объём.
Идём в лабораторию — здесь чуть сложнее
Пользуйся дополнительными формулами для вычисления.
15. К 200 г воды добавили 0,5 моль хлорида натрия (NaCl). Найдите массу полученного раствора. (229,25 г)
16. Через 500 г воды пропустили 2,24 л аммиака (NH₃) (н.у.), и весь газ растворился. Найдите массу полученного раствора. (501,7 г)
17. 150 граммах воды растворили образец сахара, содержащий 1,204‧10²⁴ молекул сахарозы C₁₂H₂₂O₁₁. Найдите массу полученного раствора. (834 г)
18. В 230 мл воды растворили порцию хлорида калия, содержащую 9,03×10²² атомов калия. Найдите массу полученного раствора. (241,175 г)
19. В лаборатории для приготовления водного раствора сульфата натрия соль растворили в воде. В результате получился раствор, содержащий 3.01×10²³ атомов натрия и 6.02×10²⁴ атомов водорода. Какова масса полученного раствора? (125,5 г)
20. При подготовке раствора для проведения анализа в 1 дм³ воды растворили 150 г сульфата железа (III). Определите массу сульфат-ионов (SO₄²⁻), содержащихся в этом объёме раствора. (108 г)
21. Для приготовления раствора взяли 7,575 г нитрата калия. Какой объём воды (в см³) потребуется, если количество вещества воды должно быть в 8 раз больше, чем количество вещества соли? (Считать, что плотность воды равна 1 г/см³.) (10,8 см³)
Отлично, можем двигаться дальше.
Глава 2. Массовая доля = процентная концентрация? Да, и это не страшно!
«Да, массовая доля — это проценты. Паниковать не надо. Но считать всё равно придётся.»
— Задача по химии, практикует пассивную агрессию с формулами
Главные формулы (дополнительные формулы смотри выше):
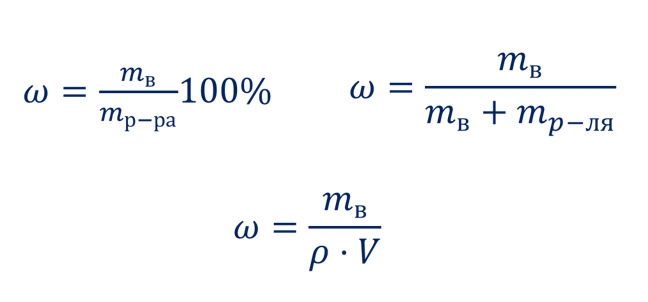
Обрати внимание! При вычислении долей округляй до 4-х знаков после запятой, соблюдая математические правила. И только потом умножай на 100%.
Пример. В стакан налили воду и высыпали 12 г сахарозы. Масса полученного раствора составила 250 г. Определите массовую долю сахарозы в растворе.
Решение: ω (сахарозы) = (12 / 250) × 100% = 4,8%. Ответ: 4,8%.
22. В 180 г водного раствора содержится 36 г мочевины. Вычислите массовую долю мочевины в растворе. (20%)
23. В одном литре воды растворили 1,75 моль гидроксида натрия. Определите массовую долю NaOH в растворе. (6,54%)
24. В 10,5 моль воды растворили 0,35 моль гидроксида калия. Рассчитайте массовую долю KOH в полученном растворе. (9,39%)
25. В 112 мл воды растворили 11,2 л газообразного аммиака (н.у.). Вычислите массовую долю NH3 в полученном растворе. (7,05%)
26. В 1 л воды растворили 60,8 л хлороводорода (н.у.). Определите массовую долю HCl в полученном растворе. (9,02%)
27. В 100 мл воды растворили 6,02·1022 молекул бромоводорода (н.у.). Вычислите массовую долю кислоты в полученном растворе. (3,52%)
28. В каком объёме воды надо растворить 30 г поваренной соли, чтобы получить 15%-ный раствор? (170 мл)
29. Какую массу хлорида бария необходимо растворить в 60 мл воды для получения 15%-ного раствора? (10,59 г)
30. Сколько граммов кристаллического йода необходимо растворить в 50 мл этилового спирта (ρсп = 0,79 г/мл), чтобы получить раствор с массовой долей йода 5% (медицинский спиртовой раствор йода)? (2,08 г)
31. Вычислите массы хлорида натрия и воды, необходимые для приготовления 0,5 л 12%-ного раствора (ρ = 1,09 г/мл). (65,4 г; 479,6 г)
32. В 1 дм3 спирта (ρ = 0,8 г/см3) растворили сероводород объемом 10 дм3 (н.у.). Определите массовую долю (%) H₂S в полученном растворе. (1,86%)
33. Чтобы получить раствор Люголя для смазывания горла при ангине, надо к 17 мл воды прибавить 1г йода и 2 г йодида калия. Рассчитайте массовые доли йода и йодида калия в растворе Люголя. (5%; 10%)
Блиц-практика



Бесплатный фрагмент закончился.
Купите книгу, чтобы продолжить чтение.