
Бесплатный фрагмент - Микрофлора кишечника и зрение
Дисклеймер
Эта книга предназначена для информационных и образовательных целей. В ней представлены современные научные данные о связи между кишечной микробиотой, системным воспалением и здоровьем глаз, а также практические рекомендации по диете, образу жизни и коррекции микробиоты.
Книга не является медицинским пособием, руководством по самодиагностике или самолечению. Она не заменяет консультацию врача-офтальмолога, гастроэнтеролога, терапевта или других профильных специалистов.
Если у вас диагностированы глазные заболевания (включая, но не ограничиваясь: катаракта, глаукома, возрастная макулярная дегенерация, диабетическая ретинопатия, увеит, синдром сухого глаза), системные заболевания (сахарный диабет, аутоиммунные заболевания, воспалительные заболевания кишечника) или любые другие хронические состояния — перед началом любых изменений в диете, приёме добавок или образе жизни обязательно проконсультируйтесь с вашим лечащим врачом.
Все рекомендации, приведённые в книге (включая диетические, пробиотические и другие), носят общий характер и не учитывают ваши индивидуальные особенности, противопоказания, принимаемые лекарства или текущее состояние здоровья. Реакция на изменение диеты, приём пробиотиков или других добавок может варьироваться.
Автор и издатель не несут ответственности за возможные негативные последствия самостоятельного применения описанных методов без предварительной консультации с квалифицированным медицинским специалистом.
Особую осторожность следует соблюдать:
— при беременности и грудном вскармливании;
— при тяжёлых иммунодефицитах (включая химиотерапию, трансплантацию органов);
— при острых инфекционных заболеваниях;
— при приёме антикоагулянтов (препаратов, разжижающих кровь);
— при тяжёлых заболеваниях печени и почек.
Регулярные профилактические осмотры у офтальмолога, а при наличии кишечных симптомов — у гастроэнтеролога, остаются обязательной частью заботы о здоровье. Осознанный подход, сочетание информации из этой книги с профессиональной медицинской поддержкой — лучший путь к сохранению зрения и общего здоровья.
Введение
Почему офтальмолог не смотрит в кишечник
Ось «кишечник — глаза»: скрытая связь, меняющая подход к лечению
Представьте себе типичный прием у офтальмолога. Пациент жалуется на сухость, жжение, нечеткое зрение, быструю утомляемость глаз. Врач закапывает капли, расширяющие зрачок, смотрит в глазное дно, измеряет внутриглазное давление. Диагнозы звучат привычно: синдром сухого глаза, начальная катаракта, фоновая ретинопатия. Назначения тоже стандартны: увлажняющие капли, возможно, противовоспалительные, витамины для глаз.
И лишь один вопрос почти никогда не звучит: «А как у вас дела с животом?»
Это не случайность и не невнимательность. Так сложилась медицинская культура: глаз — это отдельный орган, а кишечник — совсем другая история, для гастроэнтеролога. Веками офтальмология развивалась как высокотехнологичная специальность, оперирующая микроскопами, лазерами и искусственными хрусталиками. В этой парадигме кишечник казался бесконечно далеким.
Но наука последних десяти лет говорит обратное.
Кишечник — не просто пищеварительная труба
Примерно 100 триллионов микроорганизмов живут внутри каждого из нас. Их совокупный геном (микробиом) в 150 раз больше человеческого. Эти бактерии, грибы и вирусы не просто переваривают клетчатку — они управляют нашим иммунитетом, синтезируют нейромедиаторы, влияют на настроение, вес и — как сейчас выясняется — на зрение.
Ось «кишечник — мозг» уже стала мейнстримом. Ось «кишечник — глаза» только входит в науку, но данные накапливаются с пугающей быстротой.
Вот лишь несколько фактов, которые меняют привычную картину:
— Пациенты с синдромом сухого глаза в три раза чаще страдают синдромом раздраженного кишечника. Их объединяет не случайность, а общий механизм — низкоинтенсивное системное воспаление, источник которого часто находится именно в кишечнике.
— При возрастной макулярной дегенерации (главной причине слепоты у пожилых) в крови повышены уровни бактериального эндотоксина — липополисахарида (LPS). Этот токсин просачивается через «дырявый» кишечный барьер и запускает хроническое воспаление в сетчатке.
— Экспериментальное введение пробиотиков мышам с увеитом (воспалением сосудистой оболочки глаза) уменьшает тяжесть заболевания в 2–3 раза. А трансплантация фекальной микробиоты от здоровых доноров способна остановить прогрессирование болезни.
Почему же мы не ищем причину в кишечнике?
Три главных препятствия.
Первое — инерция мышления. Врачей учили: глазное заболевание лечат в глазу. Капли, инъекции, лазер, операция. Мысль о том, что хронический блефарит может быть следствием дисбиоза тонкой кишки, до сих пор кажется ересью.
Второе — разрыв между специальностями. Офтальмолог не назначает анализ кала, а гастроэнтеролог не смотрит в глазное дно. Клинические рекомендации существуют внутри каждой дисциплины, и почти нигде нет пункта «исключить патологию кишечника».
Третье — сложность доказательств. Связь между микробиотой и глазом редко бывает прямой. Это всегда цепочка: дисбиоз → нарушение барьера → эндотоксемия → системное воспаление → поражение тканей глаза. Доказать причинно-следственные связи в такой системе сложно, и скептики всегда могут сказать: «это просто корреляция».
Но корреляция, повторяющаяся в десятках исследований, перестает быть случайностью.
Что вы узнаете из этой книги
Мы не будем утверждать, что все болезни глаз лечатся через кишечник. Это было бы наивно и нечестно. Но мы покажем, что значительная часть хронических офтальмологических заболеваний имеет кишечный компонент, который сегодня почти всегда игнорируется.
В первой части мы разберем механизмы: как бактерии, их метаболиты и иммунные сигналы путешествуют из кишечника к сетчатке.
Во второй части пройдем по конкретным болезням — от сухого глаза до макулярной дегенерации и близорукости — и посмотрим на них через призму микробиоты.
В третьей части ответим на главный практический вопрос: что делать? Какие анализы сдать, какие пробиотики работают (а какие — нет), как изменить диету и стоит ли всерьез рассматривать фекальную трансплантацию.
Важное предупреждение
Эта книга — не призыв отказаться от офтальмолога в пользу гастроэнтеролога. Капли, лазер и хирургия остаются незаменимыми там, где они нужны. Но если вы или ваш пациент годами лечите синдром сухого глаза без успеха, если возрастная макулярная дегенерация прогрессирует вопреки терапии, если диабетическая ретинопатия ведет себя агрессивно — возможно, пора задать тот самый вопрос.
Как у вас с животом?
Ось «кишечник — глаза» реальна. Скрытая связь существует. И игнорировать ее сегодня — значит упускать возможность помочь пациентам там, где стандартные подходы исчерпали себя.
Давайте разбираться.
Часть 1. Механизмы связи: от микробиома к сетчатке
Глава 1. Кишечная микрофлора как невидимый орган
1.1. Состав, здоровый микробиом и дисбиоз
Представьте, что внутри вас живёт целый город. Не маленькая деревня, а мегаполис с населением под сто триллионов жителей. Эти жители — бактерии, археи, грибы и вирусы. Вместе они весят от одного до двух килограммов — примерно как мозг взрослого человека.
Это и есть кишечная микробиота.
Долгое время мы относились к ней как к попутчикам: мол, живут себе в толстой кишке, переваривают остатки пищи, и ладно. Но за последние два десятилетия взгляд перевернулся. Микробиоту всё чаще называют «невидимым органом» — и вот почему.
У неё есть все признаки настоящего органа: она имеет определённый состав, выполняет сотни биохимических реакций, взаимодействует с другими системами тела и… может болеть. А когда болеет она — страдает весь организм, включая глаза.
Кто живёт внутри нас
Если заглянуть в здоровую толстую кишку, мы увидим удивительное разнообразие. Более 90% микробиоты составляют бактерии всего двух типов (филумов): Firmicutes и Bacteroidetes. Остальное — Actinobacteria, Proteobacteria, Verrucomicrobia и другие.
Но внутри этих типов — тысячи видов. Идеальный микробиом похож на тропический лес: чем больше видов, тем он устойчивее.
Вот основные «профессии» этих микроорганизмов:
— Ферментация клетчатки. Бактерии расщепляют то, что не переварили наши собственные ферменты, и производят короткоцепочечные жирные кислоты (КЦЖК) — главное топливо для клеток кишечника.
— Синтез витаминов. Микробиота производит витамины К, группы В (биотин, фолиевую кислоту, В12).
— Защита от патогенов. Полезные бактерии занимают места и поедают ресурсы, не оставляя шансов сальмонелле или клостридиям.
— Обучение иммунной системы. С первых дней жизни микробиота «тренирует» иммунитет, показывая, на что стоит реагировать, а на что — нет.
Что такое здоровый микробиом
Здоровье микробиоты — это не какой-то один «правильный» набор бактерий. Два совершенно здоровых человека могут иметь очень разный состав микробиома. Тем не менее учёные выделяют три ключевых признака здоровья.
1. Высокое разнообразие.
Чем больше разных видов живёт в кишечнике, тем устойчивее система. Если какой-то вид пострадает (например, после антибиотиков), другие его подстрахуют. Низкое разнообразие — маркер проблем: оно характерно для ожирения, воспалительных заболеваний кишечника и даже депрессии.
2. Стабильность во времени.
Здоровый микробиом не прыгает от недели к неделе. Он меняется медленно — с возрастом, с кардинальной сменой диеты, после болезней. Если состав скачет без видимой причины — это признак нестабильности.
3. Резистентность к патогенам.
Хороший микробиом — это крепость. Он не позволяет чужакам закрепиться. Это называется колонизационной резистентностью. Чем она выше, тем меньше риск кишечных инфекций.
Дисбиоз: когда баланс нарушен
Дисбиоз — это не просто слово. Это состояние, при котором микробиота перестаёт быть другом. Меняется состав, падает разнообразие, исчезают полезные виды и разрастаются вредные.
Представьте тот же тропический лес, в котором вырубили половину деревьев и засеяли поле борщевиком. Экосистема рухнула.
Дисбиоз бывает разным.
По составу:
— Дефицит полезных бактерий — мало Firmicutes, мало Faecalibacterium prausnitzii (главного производителя бутирата).
— Избыток условно-патогенных — рост Proteobacteria (например, кишечной палочки), стрептококков, стафилококков.
— Общее падение разнообразия — самое тревожное состояние.
По причинам:
— Антибиотики — главный истребитель микробиоты. Курс антибиотиков может уничтожить до трети видов, и некоторые не восстанавливаются годами.
— Диета — недостаток клетчатки, обилие сахара, насыщенных жиров и эмульгаторов.
— Стресс — хронический стресс меняет состав микробиоты через нервную систему и гормоны.
— Инфекции и болезни — и наоборот: дисбиоз может быть и причиной, и следствием.
По последствиям:
А вот здесь начинается самое интересное для нашей темы. Дисбиоз почти всегда ведёт к двум вещам:
— Нарушению кишечного барьера — о нём мы поговорим в следующей подглаве.
— Хроническому системному воспалению — которое бьёт по всем органам, включая глаза.
Как узнать, есть ли у вас дисбиоз?
К сожалению, у дисбиоза нет одного «золотого» симптома. Но есть косвенные признаки, которые должны насторожить:
— Регулярные вздутия, метеоризм, запоры или диарея без явной причины.
— Непереносимость продуктов, которой раньше не было.
— Частые простуды и инфекции — намёк на ослабленный иммунитет.
— Усталость, туман в голове, плохое настроение — ось «кишечник–мозг» работает в обе стороны.
И, как мы увидим в части 2 этой книги, — хронические заболевания глаз, которые плохо поддаются лечению.
Точный диагноз можно поставить только с помощью анализа кала (об этом — в главе 7). Но даже без анализов понятно одно: образ жизни, который вредит кишечнику, рано или поздно навредит и зрению.
Ключевые выводы подглавы 1.1
— Кишечная микробиота — это не просто «бактерии в животе», а полноценный орган массой 1–2 кг.
— Здоровый микробиом разнообразен, стабилен и устойчив к патогенам.
— Дисбиоз — нарушение этого баланса — ведёт к снижению защиты, нарушению барьера и хроническому воспалению.
— Причины дисбиоза: антибиотики, бедная клетчаткой диета, стресс, инфекции.
— Косвенные признаки дисбиоза — кишечные симптомы, частые инфекции, усталость — а также плохо поддающиеся лечению глазные болезни.
1.2. «Дырявый кишечник»: барьерная функция и белок зонулин
Представьте себе крепостную стену. В здоровом состоянии она пропускает только то, что нужно: обученных гонцов, воду, мелкие питательные вещества. Но если в стене появляются трещины, внутрь начинают просачиваться враги, воры и мусор. Начинается хаос.
Кишечник устроен так же. Только стена здесь — это один слой эпителиальных клеток, который отделяет внутренность кишки (где живут триллионы бактерий и переваривается пища) от стерильного внутреннего мира организма.
Когда этот слой работает правильно — мы здоровы. Когда он повреждается — возникает состояние, которое называют «дырявый кишечник» (научно — повышенная кишечная проницаемость).
И это состояние напрямую связано с глазами.
Как устроен кишечный барьер
Кишечный барьер — это не просто «плёнка». Это сложная многоуровневая система.
Первый уровень — физический барьер.
Эпителиальные клетки соединяются друг с другом специальными белками — плотными контактами (tight junctions). Это своего рода застёжки-молнии между соседними клетками. Они не склеены намертво: природа предусмотрела механизмы, чтобы открывать и закрывать эти «молнии» выборочно.
Второй уровень — химический барьер.
Слизь (муцин), антимикробные пептиды, иммуноглобулин А (sIgA) — всё это нейтрализует патогены, не давая им даже приблизиться к эпителию.
Третий уровень — иммунный.
Под эпителием находится собственная пластинка слизистой (lamina propria), кишащая иммунными клетками. Они терпимы к полезным бактериям, но готовы атаковать тех, кто прорвался.
В здоровом кишечнике эти три уровня работают как швейцарские часы.
Что такое повышенная проницаемость
Проблема начинается, когда плотные контакты перестают нормально закрываться. Застёжки-молнии остаются приоткрытыми. Через щели начинают просачиваться:
— Бактериальные эндотоксины (например, липополисахарид, LPS) — фрагменты стенок погибших бактерий.
— Непереваренные фрагменты пищи.
— Сами живые бактерии (реже, но бывает).
Организм видит это как вторжение. Иммунная система реагирует бурно: выброс цитокинов, активация макрофагов, системное воспаление.
Этот процесс называется эндотоксемией — наличием бактериальных токсинов в крови.
Белок зонулин: главный дирижёр проницаемости
Долгое время было непонятно: что именно управляет плотными контактами? Почему они то открываются, то закрываются?
В 2000 году итальянский учёный Алессио Фазано сделал открытие. Он обнаружил белок, который получил название зонулин (от лат. zonula — поясок, плотный контакт).
Зонулин работает так:
— Когда в кишечнике появляются бактерии или глютен (у чувствительных людей), клетки выделяют зонулин.
— Зонулин даёт сигнал плотным контактам: «открыться».
— Проницаемость повышается — организм может быстрее получить доступ к содержимому кишечника (в случае инфекции это полезно).
Всё хорошо, пока зонулин не становится хронически повышенным. При постоянном стрессе, воспалении, дисбиозе, неправильном питании уровень зонулина остаётся высоким. Плотные контакты не закрываются полностью. И тогда «дырявый кишечник» становится хроническим состоянием.
Уровень зонулина в кале или крови — один из объективных маркеров кишечной проницаемости.
Почему это важно для глаз
Глаз, особенно сетчатка, — это иммунопривилегированный орган. То есть он защищён от избыточных иммунных атак. Но у этой защиты есть предел.
Когда из «дырявого» кишечника в кровь постоянно поступает липополисахарид (LPS), иммунная система находится в состоянии хронической боевой готовности. Цитокины циркулируют по всему организму — и достигают гемато-ретинального барьера.
Последствия:
— Хроническое низкоинтенсивное воспаление в сетчатке.
— Повреждение пигментного эпителия сетчатки (при ВМД).
— Утолщение базальной мембраны капилляров (при диабетической ретинопатии).
— Нарушение слезной пленки (при синдроме сухого глаза).
Связь не всегда прямая, но она прослеживается чётко. У пациентов с синдромом раздражённого кишечника (СРК) — классическим состоянием, связанным с повышенной проницаемостью, — синдром сухого глаза встречается в 2–3 раза чаще, чем в среднем в популяции.
Что делает кишечник «дырявым»
Факторы, повышающие проницаемость:

Можно ли восстановить барьер
Да. И это хорошая новость. Кишечный эпителий обновляется каждые 3–5 дней, и если убрать повреждающие факторы, он способен восстановиться.
Основные стратегии (подробно — в главе 8):
— Увеличить потребление клетчатки (КЦЖК питают эпителий).
— Добавить пребиотики и пробиотики (особенно Lactobacillus rhamnosus, Bifidobacterium longum).
— Исключить (хотя бы временно) сахар, эмульгаторы, алкоголь.
— Управлять стрессом — медитация, сон, физическая активность снижают зонулин.
Восстановление барьера — один из ключей к снижению системного воспаления и, как следствие, к улучшению здоровья глаз.
Ключевые выводы подглавы 1.2
— Кишечный барьер — это многоуровневая защита, ключевую роль в которой играют плотные контакты (tight junctions) между эпителиальными клетками.
— Белок зонулин регулирует открытие и закрытие плотных контактов; его хроническое повышение ведёт к «дырявому кишечнику».
— Через «дырявый» кишечник в кровь проникают эндотоксины (LPS), запуская системное воспаление.
— Системное воспаление достигает гемато-ретинального барьера и повреждает ткани глаза.
— Факторы риска: дисбиоз, глютен (у чувствительных), стресс, сахар, эмульгаторы, НПВС, алкоголь.
— Барьер восстанавливаем — через диету, пробиотики, управление стрессом.
1.3. Три ключевых метаболита: короткоцепочечные жирные кислоты, триптофан, эндотоксины
Бактерии, живущие в кишечнике, — это не просто пассажиры. Это маленькие химические фабрики. Они поглощают то, что мы съели, перерабатывают и выбрасывают в окружающее пространство десятки различных молекул.
Некоторые из этих молекул полезны для нас. Некоторые — нейтральны. Некоторые — откровенно вредны.
Для понимания связи между кишечником и глазом нужно знать три группы метаболитов. Это короткоцепочечные жирные кислоты (КЦЖК), производные триптофана и эндотоксины (липополисахарид, LPS).
Первые — наши друзья. Вторые — и друзья, и враги, в зависимости от контекста. Третьи — почти всегда враги, если попадают не туда.
Короткоцепочечные жирные кислоты (КЦЖК): главные защитники
Короткоцепочечные жирные кислоты — это то, во что бактерии превращают пищевую клетчатку. Три главные КЦЖК:
— Ацетат (C2)
— Пропионат (C3)
— Бутират (C4)
Из них самый изученный и важный — бутират.
Что делает бутират в кишечнике:
— Топливо для эпителия. Клетки толстой кишки получают до 70% энергии именно из бутирата. Без него они голодают и отмирают.
— Укрепление барьера. Бутират стимулирует синтез белков плотных контактов — тех самых «застёжек-молний».
— Противовоспалительное действие. Бутират подавляет NF-κB — главный переключатель воспаления в клетках.
А что насчёт глаз?
И вот здесь начинается самое интересное. Бутират и другие КЦЖК не остаются только в кишечнике. Они всасываются в кровь и могут достигать отдалённых органов — включая сетчатку.
Исследования последних лет показывают:
— Бутират защищает ганглиозные клетки сетчатки от гибели при экспериментальной глаукоме.
— Пропионат снижает риск возрастной макулярной дегенции в моделях на мышах.
— Пациенты с высокой долей бактерий-производителей КЦЖК (например, Faecalibacterium prausnitzii) реже страдают хроническими воспалительными заболеваниями глаз.
Коротко: чем больше клетчатки вы едите, тем больше КЦЖК производят бактерии, и тем лучше защищены ваши глаза — через снижение системного воспаления.
Триптофан: амбивалентная молекула
Триптофан — это незаменимая аминокислота. Мы получаем её из пищи (индейка, творог, орехи, бананы). И кишечные бактерии, и наши собственные клетки умеют её перерабатывать.
Проблема в том, что продукты переработки бывают очень разными.
Хороший путь: триптофан → серотонин → мелатонин
Часть триптофана превращается в серотонин («гормон счастья») и мелатонин (гормон сна). Это полезно для настроения, циркадных ритмов — и, как выясняется, для сетчатки. Мелатонин, синтезируемый в кишечнике, работает как антиоксидант и защищает фоторецепторы от светового повреждения.
Плохой путь: триптофан → кинуренин
Другая часть триптофана превращается в кинуренин. Кинуренин — нейротоксин. Он повреждает нервные клетки, включая ганглиозные клетки сетчатки. Высокий уровень кинуренина обнаруживается у пациентов с глаукомой и возрастной макулярной дегенерацией.
Что определяет, по какому пути пойдёт триптофан?
В значительной степени — микробиота. Некоторые бактерии (например, Lactobacillus) сдвигают метаболизм в сторону серотонина. Другие (например, Clostridium) — в сторону кинуренина. А хроническое воспаление (в том числе из-за «дырявого» кишечника) активирует ферменты, которые тоже толкают триптофан в токсичный путь.
Баланс триптофанового обмена — ещё один мост между кишечником и зрением.
Эндотоксины (LPS): главные вредители
Липополисахарид (LPS) — это фрагмент клеточной стенки грамотрицательных бактерий (например, E. coli, Klebsiella, Salmonella). В норме LPS остаётся в просвете кишки и не причиняет вреда.
Но когда кишечный барьер повреждён («дырявый кишечник»), LPS просачивается в кровь. Возникает состояние метаболической эндотоксемии — низкого, но хронического уровня бактериальных токсинов в крови.
Что делает LPS в организме:
— Активирует иммунные клетки через рецептор TLR4 (как пожарная тревога, которая не выключается).
— Запускает выброс провоспалительных цитокинов — IL-1, IL-6, TNF-α.
— Вызывает окислительный стресс.
А что с глазами?
Сетчатка чрезвычайно чувствительна к LPS. Даже низкие концентрации, циркулирующие в крови, со временем повреждают:
— Пигментный эпителий сетчатки — его клетки начинают гибнуть, что ведёт к макулярной дегенерации.
— Сосуды сетчатки — развивается эндотелиальная дисфункция, один из механизмов диабетической ретинопатии.
— Слезную железу — снижается выработка слезы, возникает синдром сухого глаза.
Ключевое открытие последних лет: уровень LPS в крови — независимый фактор риска прогрессирования возрастной макулярной дегенерации. И этот уровень напрямую зависит от состояния кишечного барьера.
Три метаболита: сводная таблица
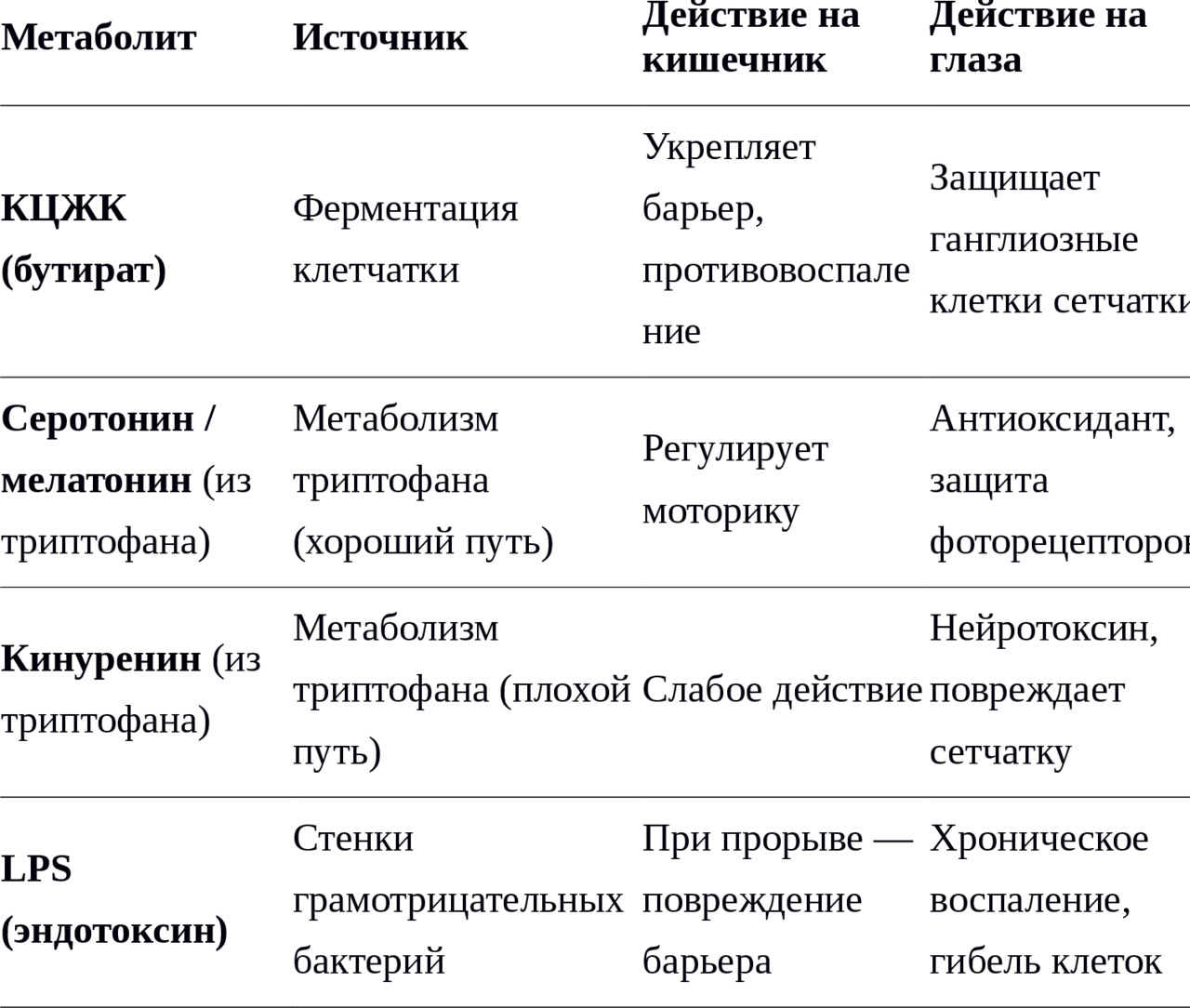
Что это значит для практики
Понимание трёх метаболитов даёт конкретные стратегии:
Чтобы повысить КЦЖК → ешьте больше клетчатки (овощи, бобовые, цельнозерновые, орехи). Чем разнообразнее растительная пища, тем разнообразнее бактерии-производители бутирата.
Чтобы триптофан шёл в хороший путь → поддерживайте здоровую микробиоту (пробиотики с Lactobacillus) и снижайте системное воспаление (лечите «дырявый» кишечник, убирайте сахар).
Чтобы снизить LPS → восстанавливайте кишечный барьер (см. подглаву 1.2) и снижайте долю грамотрицательных бактерий в микробиоте (меньше сахара, меньше насыщенных жиров).
Кишечник и глаза общаются на языке метаболитов. И мы можем научиться говорить на этом языке.
Ключевые выводы подглавы 1.3
— Короткоцепочечные жирные кислоты (особенно бутират) — защитники: укрепляют кишечный барьер и снижают воспаление в сетчатке.
— Триптофан — двуликая молекула: в здоровой микробиоте превращается в полезные серотонин и мелатонин, при воспалении — в токсичный кинуренин.
— Эндотоксины (LPS) — главные вредители: просачиваясь через «дырявый» кишечник, вызывают хроническое воспаление и повреждают сетчатку.
— Баланс этих трёх групп метаболитов определяет риск многих глазных заболеваний — от сухого глаза до макулярной дегенерации.
— Диета и образ жизни напрямую влияют на этот баланс.
Глава 2. Как кишечник разговаривает с глазом
2.1. Иммунный, метаболический и нервный пути связи
Итак, мы уже знаем, что такое микробиота, что такое дисбиоз и «дырявый кишечник», а также познакомились с тремя главными группами метаболитов — друзьями и врагами.
Но остаётся главный вопрос: как именно информация из кишки доходит до глаза?
Это не магия и не эзотерика. Это конкретные анатомические и биохимические пути, которые наука расшифровала за последние 10–15 лет.
Таких путей три:
— Иммунный путь — самый мощный и изученный.
— Метаболический путь — через кровоток, напрямую.
— Нервный путь — через блуждающий нерв и вегетативную систему.
Все три работают одновременно, переплетаются и усиливают друг друга. Давайте разберём каждый.
Иммунный путь: главная магистраль
Представьте себе систему оповещения о пожарной тревоге, которая соединяет все города страны. В кишечнике расположен главный диспетчерский пункт. Глаз — один из удалённых постов.
Что такое GALT?
В стенке кишечника находится крупнейшая в организме иммунная территория — GALT (gut-associated lymphoid tissue, кишечно-ассоциированная лимфоидная ткань). Это скопления лимфоцитов, макрофагов, дендритных клеток, которые круглосуточно мониторят содержимое кишки.
GALT решает главную задачу: отличить «своих» от «чужих».
— К полезным бактериям — терпимость.
— К патогенам — атака.
Но есть одна тонкость. Обученные в GALT иммунные клетки не остаются в кишечнике. Они путешествуют по всему организму через лимфатическую и кровеносную системы. Это называется хоминг (homing) — клетки «знают», куда им идти.
И некоторые из них направляются в глаз.
Почему глаз так уязвим?
Глаз — иммунопривилегированный орган. Это значит, что иммунные реакции в нём приглушены, чтобы не повредить тонкие структуры сетчатки. Но у этой защиты есть обратная сторона: если активированные лимфоциты из кишечника всё же проникают в глаз, они могут натворить много бед — потому что местные механизмы контроля не рассчитаны на агрессивное вторжение.
Клинический пример: увеит
Увеит — воспаление сосудистой оболочки глаза. В трети случаев его причина так и остаётся неизвестной — это называется идиопатическим увеитом.
Но исследования последних лет показывают: у многих пациентов с идиопатическим увеитом в кишечнике обнаруживается дисбиоз и повышенный уровень Bacteroides и E. coli. А лимфоциты, выделенные из глаза, несут маркеры, характерные для кишечника.
Гипотеза: кишечный дисбиоз запускает активацию T-лимфоцитов, которые по ошибке атакуют ткани глаза — потому что белки сетчатки и белки некоторых кишечных бактерий похожи. Это называется антигенной мимикрией (подробнее — в главе 4).
Коротко по иммунному пути:
Дисбиоз → активация лимфоцитов в GALT → миграция лимфоцитов в глаз → хроническое воспаление → повреждение сетчатки или сосудистой оболочки.
Метаболический путь: химическая почта
Иммунный путь — это клетки. Метаболический путь — это молекулы.
Мы уже говорили о КЦЖК, триптофане и LPS в подглаве 1.3. Теперь посмотрим, как они физически добираются до глаза.
Маршрут простой:
Кишечник → воротная вена → печень (часть метаболитов здесь задерживается и обезвреживается) → общий кровоток → гемато-ретинальный барьер → сетчатка.
Что проходит через этот фильтр?
— Короткоцепочечные жирные кислоты проходят легко. Они маленькие и водорастворимые. Бутират из кишечника может быть обнаружен в стекловидном теле глаза через 30–60 минут после приёма пищи, богатой клетчаткой.
— Производные триптофана — тоже. Серотонин и кинуренин свободно циркулируют в крови и влияют на сетчатку. Именно поэтому уровень кинуренина в крови коррелирует с тяжестью глаукомы.
— LPS (эндотоксин) — крупная молекула. В норме печень задерживает большую часть LPS из воротной вены. Но если «дырявый» кишечник пропускает слишком много токсина, печень не справляется. LPS попадает в общий кровоток и достигает гемато-ретинального барьера. А там запускает локальное воспаление через рецепторы TLR4, которые есть на клетках пигментного эпителия сетчатки.
Ключевое отличие метаболического пути от иммунного:
Иммунный путь требует времени (дни и недели на активацию и миграцию клеток). Метаболический путь — быстрый. Часы, иногда минуты. Съели что-то не то — через пару часов изменился состав метаболитов в крови, и сетчатка это почувствовала.
Именно этим объясняется феномен, который знают многие пациенты с сухим глазом или увеитом: после «запретной» еды (много сахара, жирного, острого) симптомы ухудшаются уже на следующий день.
Нервный путь: прямая линия
Третий путь — самый быстрый, но и самый тонкий.
Блуждающий нерв (nervus vagus) — главный коммуникатор между кишечником и мозгом. Он передаёт сигналы о растяжении стенки кишки, о химическом составе химуса, о присутствии бактерий.
Но блуждающий нерв не идёт напрямую к глазу. Его терминалы — в стволе мозга. А оттуда сигналы могут передаваться дальше, в том числе к глазодвигательным нервам и к вегетативным центрам, регулирующим слезопродукцию и тонус сосудов глаза.
Что именно передаётся по нервам?
— Рефлекторные сигналы. Например, раздражение кишечника при пищевом отравлении может через блуждающий нерв вызвать сужение зрачка или изменение внутриглазного давления.
— Воспалительный рефлекс. Это открытие последних 20 лет: блуждающий нерв может тормозить воспаление через выброс ацетилхолина, который связывается с рецепторами на иммунных клетках и «успокаивает» их. Этот механизм работает и в кишечнике, и в глазу. Хронический стресс (который подавляет тонус блуждающего нерва) ослабляет этот противовоспалительный рефлекс — и глаз становится более уязвимым.
Есть ли доказательства?
Да. Эксперименты на животных показывают:
— Перерезка блуждающего нерва у мышей утяжеляет течение экспериментального увеита.
— Электрическая стимуляция блуждающего нерва, наоборот, снижает воспаление в сетчатке.
— Пациенты с синдромом сухого глаза и низким тонусом блуждающего нерва (измеряемым по вариабельности сердечного ритма) хуже отвечают на стандартную терапию.
Нервный путь — это не главная магистраль, но важный модулятор. Он может усиливать или ослаблять эффекты двух других путей.
Три пути в одной таблице

Что это значит на практике
Понимание трёх путей даёт три стратегии вмешательства:
— Через иммунный путь — восстанавливать микробиоту, снижать дисбиоз, чтобы не активировать «неправильные» лимфоциты. Это долгая стратегия (месяцы).
— Через метаболический путь — корректировать диету здесь и сейчас. Больше клетчатки (КЦЖК), меньше сахара и насыщенных жиров (LPS и кинуренин). Эффект может наступить через дни–недели.
— Через нервный путь — управлять стрессом, улучшать тонус блуждающего нерва (дыхательные практики, медитация, физическая активность, холодовая стимуляция). Это усиливает противовоспалительную защиту глаза.
Лучшая стратегия — работать со всеми тремя путями одновременно.
Ключевые выводы подглавы 2.1
— Кишечник и глаз связаны тремя независимыми, но взаимодополняющими путями: иммунным, метаболическим и нервным.
— Иммунный путь — главный: активированные в GALT лимфоциты мигрируют в глаз и могут вызывать хроническое воспаление (увеит, сухой глаз).
— Метаболический путь — быстрый: КЦЖК, триптофан и LPS напрямую циркулируют в крови и воздействуют на сетчатку.
— Нервный путь — модулятор: блуждающий нерв может тормозить воспаление в глазу; стресс ослабляет этот механизм.
— Лечение глазных заболеваний через кишечник должно учитывать все три пути одновременно.
2.2. Сходство барьеров: кишечный эпителий и гемато-ретинальный барьер
На первый взгляд, кишечник и глаз не имеют ничего общего. Один — трубка длиной несколько метров, заполненная пищей и бактериями. Другой — изящный оптический прибор размером с виноградину.
Но если посмотреть на них под микроскопом, обнаруживается поразительное сходство. И кишечник, и глаз защищены от внешнего мира барьерами, которые устроены по одному и тому же принципу.
Понимание этого сходства — ключ к разгадке того, почему проблемы в одном органе так легко перекидываются на другой.
Два барьера, один чертёж
Кишечный барьер (мы уже говорили о нём в главе 1.2) отделяет просвет кишки (где живут триллионы бактерий) от стерильного внутреннего пространства организма.
Гемато-ретинальный барьер (ГРБ) отделяет кровеносные сосуды сетчатки от нервной ткани глаза. Он не пропускает лишние молекулы и клетки в сетчатку, потому что любое воспаление здесь может привести к необратимой потере зрения.
Что у них общего?
1. Оба состоят из одного слоя клеток.
— Кишечный барьер — один слой энтероцитов.
— Гемато-ретинальный барьер — один слой эндотелиальных клеток сосудов сетчатки (внутренняя часть) или один слой клеток пигментного эпителия сетчатки (внешняя часть).
2. Оба используют плотные контакты (tight junctions).
Те самые «застёжки-молнии», о которых мы говорили в подглаве 1.2, соединяют соседние клетки и регулируют проницаемость. В кишечнике их открывает белок зонулин. В глазу тоже есть аналогичные регуляторы.
3. Оба имеют иммунную «подстраховку».
Под кишечным эпителием — собственный слой слизистой с иммунными клетками. Под гемато-ретинальным барьером — микроглия (собственные иммунные клетки сетчатки) и система комплемента.
4. Оба страдают от одних и тех же врагов.
Хроническое воспаление, окислительный стресс, высокий уровень сахара в крови — всё это повреждает и кишечный барьер, и гемато-ретинальный. И тот, и другой становятся «дырявыми».
Параллель: «дырявый кишечник» и «дырявая сетчатка»
Если кишечный барьер повреждается, возникает состояние, которое мы называем «дырявый кишечник». Через него в кровь просачиваются эндотоксины, бактерии, непереваренные фрагменты пищи.
Аналогично, если повреждается гемато-ретинальный барьер, сетчатка становится уязвимой. В неё проникают:
— Цитокины из крови (которые там появились из-за «дырявого» кишечника).
— Иммунные клетки (которые ошибочно атакуют нейроны сетчатки).
— Токсичные молекулы (например, кинуренин).
Клинический пример: диабетическая ретинопатия
При диабете высокий уровень глюкозы в крови повреждает оба барьера.
— В кишечнике: повышается проницаемость, растёт уровень LPS в крови (эндотоксемия).
— В сетчатке: повреждаются плотные контакты эндотелия сосудов, белки-застёжки «расстёгиваются», и в сетчатку начинают просачиваться жидкость и белки. Это называется макулярный отёк — одна из главных причин слепоты при диабете.
Лечение, которое восстанавливает кишечный барьер (диета, пробиотики, снижение воспаления), в экспериментах на животных замедляет и повреждение гемато-ретинального барьера.
Общие регуляторы: что разрушает оба барьера
Наука выделяет несколько универсальных механизмов, которые повреждают и кишечный барьер, и гемато-ретинальный барьер.


Что важно: Повреждение одного барьера ускоряет повреждение другого.
«Дырявый» кишечник → эндотоксемия → системное воспаление → повреждение гемато-ретинального барьера. Это порочный круг, который нужно разрывать с обеих сторон.
Общие защитники: что укрепляет оба барьера
Хорошая новость: стратегии, которые укрепляют кишечный барьер, в большинстве случаев укрепляют и гемато-ретинальный барьер.

Клинический вывод
Сходство барьеров объясняет, почему пациенты с хроническими кишечными заболеваниями (синдром раздражённого кишечника, болезнь Крона, целиакия) имеют повышенный риск глазных патологий — и наоборот.
Если вы лечите глаз, не забывайте про кишечник. Восстановление кишечного барьера — это не «альтернативная медицина», а патогенетически обоснованный подход к защите сетчатки.
И наоборот: если у пациента с ВМД или диабетической ретинопатией прогрессирование не удаётся остановить стандартной терапией — имеет смысл проверить состояние кишечного барьера (анализ на зонулин, LPS, маркеры воспаления).
Ключевые выводы подглавы 2.2
— Кишечный барьер и гемато-ретинальный барьер устроены по одному принципу: один слой клеток + плотные контакты + иммунная поддержка.
— Факторы, повреждающие один барьер (воспаление, окислительный стресс, высокий сахар, LPS, стресс), повреждают и другой.
— «Дырявый кишечник» → эндотоксемия → системное воспаление → «дырявая сетчатка». Это порочный круг.
— Стратегии, укрепляющие кишечный барьер (бутират, витамин D, омега-3, пробиотики, полифенолы), одновременно защищают и гемато-ретинальный барьер.
— Восстановление кишечного барьера — патогенетически обоснованный метод защиты зрения при хронических воспалительных заболеваниях глаз.
2.3. Системное воспаление и окислительный стресс как общий язык
Мы разобрали три пути связи (иммунный, метаболический, нервный) и сходство двух барьеров (кишечного и гемато-ретинального). Теперь остаётся ответить на главный вопрос: что именно передаётся по этим путям? Что за сигнал идёт из больного кишечника в сетчатку?
Ответ короткий и неприятный: воспаление и окислительный стресс.
Это два универсальных языка, на которых организм сообщает сам себе: «что-то пошло не так». И если воспаление становится хроническим, а окислительный стресс — постоянным, страдают все органы. Глаз — один из самых уязвимых.
Системное воспаление: пожар, который не тушат
Воспаление — это нормальная защитная реакция. Порезали палец — появилось покраснение, отёк, боль. Это хорошо: организм борется с инфекцией и запускает заживление.
Но есть другой тип воспаления — хроническое низкоинтенсивное. Пожар, который не тушат. Он не даёт явных симптомов вроде температуры или боли, но тлеет годами, разрушая ткани понемногу каждый день.
Именно такой тип воспаления связывает кишечник и глаза.
Как это выглядит в цифрах:
У здорового человека уровень С-реактивного белка (СРБ) — классического маркера воспаления — обычно ниже 1 мг/л. При хроническом низкоинтенсивном воспалении он держится в диапазоне 1–5 мг/л. Казалось бы, немного. Но эпидемиологические исследования показывают: даже такое «лёгкое» повышение СРБ удваивает риск возрастной макулярной дегенерации.
Откуда берётся хроническое воспаление?
В контексте нашей книги — из кишечника. Конкретные механизмы:
— LPS-эндотоксемия (см. подглаву 1.3). Бактериальные токсины просачиваются через «дырявый» кишечник, попадают в кровь и активируют иммунные клетки через рецепторы TLR4.
— Дисбиотическая активация T-клеток (см. подглаву 2.1). Некоторые лимфоциты, обученные в кишечнике, становятся агрессивными и атакуют ткани по всему организму.
— Нарушение метаболизма триптофана (см. подглаву 1.3). Воспаление сдвигает обмен триптофана в сторону токсичного кинуренина, который сам по себе усиливает воспаление — порочный круг.
Что это означает для глаза:
Сетчатка — одна из самых метаболически активных тканей организма. Она потребляет кислорода больше, чем любой другой орган в пересчёте на грамм ткани. И она чрезвычайно чувствительна к воспалению.
Хроническое системное воспаление приводит к:
— Активации микроглии — собственных иммунных клеток сетчатки. Они начинают выделять провоспалительные цитокины прямо внутри глаза.
— Повреждению гемато-ретинального барьера — сетчатка теряет защиту.
— Гибели нейронов — ганглиозные клетки сетчатки (при глаукоме) и фоторецепторы (при ВМД) отмирают быстрее.
Окислительный стресс: ржавчина внутри нас
Если воспаление — это пожар, то окислительный стресс — это ржавчина. И то и другое разрушает, но разными способами.
Что такое окислительный стресс простыми словами:
В каждой клетке постоянно образуются активные формы кислорода (АФК) — агрессивные молекулы, которые повреждают белки, жиры и ДНК. В норме у клетки есть антиоксидантная защита, которая нейтрализует АФК.
Окислительный стресс — это когда АФК становится слишком много или антиоксидантная защита слабеет. Клетка начинает «ржаветь» изнутри.
Откуда берётся окислительный стресс в кишечнике:
— Воспаление само по себе генерирует АФК (иммунные клетки используют их как оружие).
— Дисбиоз: некоторые бактерии производят токсины, усиливающие окислительный стресс.
— LPS активирует фермент НАДФН-оксидазу в клетках кишечника — мощный генератор АФК.
— Неправильное питание (много сахара, трансжиров, мало антиоксидантов).
Как окислительный стресс добирается до глаза:
Во-первых, АФК из кишечника не путешествуют по крови — они слишком нестабильны. Но они повреждают кишечный барьер (усиливая «дырявость») и запускают воспаление. А воспаление уже бьёт по сетчатке.
Во-вторых, продукты окислительного стресса (например, малоновый диальдегид, 4-гидроксиноненаль) могут циркулировать в крови и напрямую повреждать клетки сетчатки.
В-третьих, окислительный стресс в кишечнике истощает общие антиоксидантные резервы организма. Глазу просто не хватает защиты.
Почему сетчатка особенно уязвима:
— В сетчатке очень высокое содержание полиненасыщенных жирных кислот (особенно докозагексаеновой кислоты, ДГК). Они необходимы для работы фоторецепторов, но чрезвычайно чувствительны к окислению.
— Сетчатка постоянно подвергается воздействию света — а свет сам по себе генерирует АФК.
— Пигментный эпителий сетчатки (ПЭС) работает на пределе: он ежедневно перерабатывает огромное количество отходов (внешние сегменты фоторецепторов) и очень чувствителен к окислительному стрессу.
Клинический пример: возрастная макулярная дегенерация
ВМД — классическая болезнь окислительного стресса. В сетчатке пациентов с ВМД обнаруживаются высокие уровни маркеров окисления липидов. А одним из факторов риска является низкое потребление антиоксидантов (лютеина, зеаксантина, витаминов C и E).
Теперь связь с кишечником: хроническое системное воспаление и окислительный стресс из кишечника истощают антиоксидантную защиту сетчатки и ускоряют гибель пигментного эпителия. Восстановление кишечного барьера и снижение окислительного стресса в кишечнике — это способ защитить сетчатку «с тыла».
Воспаление и окислительный стресс: два близнеца
На самом деле воспаление и окислительный стресс неразделимы. Они подпитывают друг друга:
Воспаление → иммунные клетки выделяют АФК → окислительный стресс
Окислительный стресс → повреждение клеток → выделение сигналов «помогите» → усиление воспаления
Это называется окислительно-воспалительным каскадом. Разорвать его можно только с двух сторон одновременно.
Что это значит для практики
Понимание того, что общий язык между кишечником и глазом — это воспаление и окислительный стресс, даёт конкретные терапевтические мишени.
Чтобы снизить системное воспаление (из кишечника):
— Убрать провоспалительные продукты: сахар, рафинированные масла, трансжиры, эмульгаторы.
— Добавить противовоспалительные: омега-3 (жирная рыба, льняное масло), куркумин, полифенолы.
— Восстановить кишечный барьер (см. подглаву 1.2).
— Лечить дисбиоз (пробиотики, пребиотики).
Чтобы снизить окислительный стресс (и в кишечнике, и в глазу):
— Есть продукты, богатые антиоксидантами: яркие овощи и фрукты (особенно зелёные листовые, ягоды, морковь, тыква).
— Добавить специфические для глаз антиоксиданты: лютеин и зеаксантин (шпинат, капуста кейл, яичные желтки).
— Избегать прооксидантных факторов: курения, избыточного ультрафиолета, хронического стресса.
Главный вывод: когда вы лечите кишечник (диетой, пробиотиками, восстановлением барьера), вы не просто улучшаете пищеварение. Вы снижаете уровень системного воспаления и окислительного стресса во всём организме — и сетчатка получает мощную защиту.
Ключевые выводы подглавы 2.3
— Хроническое низкоинтенсивное воспаление и окислительный стресс — два универсальных языка, на которых кишечник сообщает о своих проблемах глазу.
— Дисбиоз и «дырявый» кишечник → LPS-эндотоксемия → системное воспаление → повреждение сетчатки.
— Воспаление и окислительный стресс подпитывают друг друга, создавая порочный круг.
— Сетчатка особенно уязвима из-за высокого содержания полиненасыщенных жирных кислот, постоянного воздействия света и высокой метаболической активности.
— Снижение системного воспаления и окислительного стресса через восстановление кишечника — патогенетически обоснованный метод защиты зрения.
— Диета, богатая антиоксидантами и противовоспалительными компонентами, работает одновременно на кишечник и на глаза.
Глава 3. От дисбиоза к поражению сетчатки: цепочка событий
3.1. Нарушение барьера → эндотоксемия → активация иммунитета
Первые две главы мы закладывали фундамент. Говорили о микробиоте, о барьерах, о метаболитах, о трёх путях связи, о воспалении и окислительном стрессе.
Теперь пришло время соединить всё в единую цепочку.
Цепочка событий — это последовательность шагов, которая запускается в кишечнике, а заканчивается поражением сетчатки. Она объясняет, почему дисбиоз может привести к слепоте — и где можно вмешаться, чтобы разорвать этот путь.
В этой подглаве мы разберём первые три звена:
— Нарушение кишечного барьера («дырявый кишечник»)
— Эндотоксемия (попадание бактериальных токсинов в кровь)
— Активация системного иммунитета (пожар, который не тушат)
Звено 1: Нарушение кишечного барьера
Всё начинается здесь.
В здоровом кишечнике плотные контакты (tight junctions) надёжно закрыты. Эпителиальный слой — как хорошо уложенная брусчатка: ни одна бактерия, ни одна крупная молекула не может просочиться между клетками.
Но под воздействием факторов, которые мы перечислили в подглаве 1.2 (дисбиоз, неправильное питание, стресс, НПВС, алкоголь, инфекции), брусчатка расшатывается.
Что именно происходит:
— Белок зонулин (или его аналоги у человека) повышается в крови и в тканях кишечника.
— Зонулин даёт сигнал плотным контактам: «открыться».
— Межклеточные промежутки расширяются.
— Через образовавшиеся «щели» начинает просачиваться содержимое кишки.
Что просачивается:
— Липополисахарид (LPS) — фрагмент стенок грамотрицательных бактерий. Это главный «плохой парень».
— Бактериальная ДНК — тоже иммуногенный сигнал.
— Непереваренные фрагменты пищи — особенно глютен (у чувствительных людей) и некоторые белки.
— Живые бактерии (реже, но бывает — называется бактериальная транслокация).
Кишечный барьер больше не выполняет свою главную функцию — защищать внутреннюю среду организма от внешней. Крепость пала.
Клинические маркеры этого звена:
— Повышенный уровень зонулина в кале или крови.
— Повышенный уровень полипептида, связывающего липополисахарид (LBP) — белка, который транспортирует LPS в крови.
— Повышенная проницаемость в тесте с лактулозой/маннитом (специальный диагностический тест, который, правда, редко используется в рутинной практике).
Звено 2: Эндотоксемия
Когда LPS и другие бактериальные молекулы просачиваются через «дырявый» кишечник, они попадают в воротную вену и направляются в печень.
Печень — первая линия обороны.
В норме печень перехватывает и обезвреживает большую часть LPS. Клетки Купфера (печёночные макрофаги) захватывают токсин и разрушают его. Если количество LPS невелико, организм справляется без последствий.
Но когда «дырявый» кишечник пропускает LPS постоянно и в больших количествах, печень перегружается. Часть LPS минует печёночный фильтр и попадает в общий кровоток.
Это состояние называется метаболической эндотоксемией.
Важное уточнение: это не сепсис. При сепсисе уровень LPS в крови огромен, у пациента лихорадка, падает давление, отказывают органы. При метаболической эндотоксемии уровень LPS низкий (в 100–1000 раз ниже, чем при сепсисе), но он держится годами. Клинически это может никак не проявляться — или проявляться хронической усталостью, «туманом в голове», склонностью к простудам.
Что показывает наука:
— У людей с ожирением и диабетом 2 типа уровень LPS в крови в 2–3 раза выше, чем у здоровых.
— У пациентов с синдромом раздражённого кишечника (СРК) — тоже выше.
— У пациентов с возрастной макулярной дегенерацией — выше, чем у здоровых сверстников того же возраста.
Эндотоксемия — это мост. Она соединяет локальную проблему в кишечнике с системным воспалением, которое бьёт по всему организму, включая глаза.
Звено 3: Активация системного иммунитета
LPS в крови — это сигнал тревоги для всего организма.
Он распознаётся иммунными клетками через специальный рецептор — TLR4 (Toll-like receptor 4). Этот рецептор есть на поверхности макрофагов, дендритных клеток, нейтрофилов — и, что важно для нас, на клетках пигментного эпителия сетчатки.
Когда LPS связывается с TLR4, внутри клетки запускается каскад реакций. Главный результат: активация транскрипционного фактора NF-κB (ядерный фактор каппа-би).
NF-κB — это «главный выключатель воспаления». Когда он активируется, клетка начинает массово производить провоспалительные цитокины:
— IL-1β (интерлейкин-1 бета) — один из самых мощных медиаторов воспаления.
— IL-6 (интерлейкин-6) — стимулирует выработку белков острой фазы в печени, включая С-реактивный белок.
— TNF-α (фактор некроза опухоли альфа) — вызывает лихорадку, апоптоз (программируемую гибель клеток), повреждение сосудов.
Эти цитокины выбрасываются в кровь и циркулируют по всему организму.
Что это означает для организма:
— Воспаление становится системным. Оно больше не ограничено кишечником.
— Повышается уровень СРБ — его можно измерить в обычном анализе крови.
— Активируются иммунные клетки во всех органах, включая микроглию сетчатки.
— Создаются условия для хронического повреждения тканей.
Что это означает для глаз:
Цитокины, циркулирующие в крови, достигают гемато-ретинального барьера. Даже если сам барьер пока цел, воспалительные сигналы проходят через него (цитокины — маленькие молекулы, они проникают легче, чем LPS).
В сетчатке происходит следующее:
— Микроглия (собственные иммунные клетки сетчатки) активируется и начинает сама производить цитокины — локальное воспаление усиливается.
— Клетки пигментного эпителия сетчатки (ПЭС) получают сигнал «опасность» и меняют свою функцию. Они перестают нормально питать фоторецепторы и убирать отходы.
— Нарушается гемато-ретинальный барьер — он становится «дырявым», как и кишечный барьер до этого.
— Ганглиозные клетки сетчатки и фоторецепторы начинают гибнуть быстрее.
Вся цепочка целиком
Теперь мы можем выстроить полную последовательность:

Важно: Эта цепочка работает медленно. Между шагом 1 и шагом 6 могут пройти годы или даже десятилетия. Но она работает всегда, если не вмешаться.
Где разорвать цепочку
У этой цепочки есть слабые места. В каждом звене мы можем вмешаться и остановить прогрессирование.

Оптимальная стратегия — работать на всех уровнях одновременно. Но самое главное — звено 1. Если восстановить кишечный барьер, поток LPS прекратится, и эндотоксемия угаснет сама собой.
Ключевые выводы подглавы 3.1
— Патогенетическая цепочка «дисбиоз → поражение сетчатки» состоит из нескольких последовательных звеньев.
— Звено 1: Нарушение кишечного барьера («дырявый кишечник») из-за дисбиоза, стресса, неправильного питания.
— Звено 2: Эндотоксемия — просачивание LPS через барьер, перегрузка печени, попадание токсина в общий кровоток.
— Звено 3: Активация системного иммунитета — LPS связывается с TLR4, запускается NF-κB, массово выделяются цитокины (IL-1β, IL-6, TNF-α).
— Цитокины достигают сетчатки, активируют микроглию, повреждают пигментный эпителий и гемато-ретинальный барьер.
— Цепочка работает медленно (годы), но неумолимо. Разорвать её можно на любом звене, но эффективнее всего — восстановив кишечный барьер.
3.2. Цитокиновое «цунами»: IL-6, TNF-α, IL-17 и их действие на глаз
В предыдущей подглаве мы остановились на том, что LPS из «дырявого» кишечника активирует иммунные клетки, и те начинают массово выбрасывать провоспалительные цитокины.
Теперь разберёмся, что это за цитокины, как они действуют и почему они так опасны для глаза.
Цитокины — это молекулярные сигналы, которыми иммунные клетки общаются друг с другом. В норме они необходимы для защиты от инфекций. Но когда их становится слишком много и они циркулируют в крови годами, они превращаются из защитников в разрушителей.
Три цитокина играют главную роль в связке «кишечник — глаза»: IL-6, TNF-α и IL-17. Их называют провоспалительными, и их повышение — маркер системного воспаления, которое бьёт по сетчатке.
IL-6: универсальный посредник
Интерлейкин-6 (IL-6) — один из самых изученных провоспалительных цитокинов. Он вырабатывается макрофагами, Т-лимфоцитами, эндотелиальными клетками, фибробластами — и, что важно, клетками пигментного эпителия сетчатки.
Что делает IL-6 в норме:
— Стимулирует иммунный ответ при инфекциях.
— Запускает выработку белков острой фазы в печени (включая СРБ).
Что делает IL-6 при хроническом повышении:
— Поддерживает хроническое воспаление.
— Повышает проницаемость сосудов (в том числе в сетчатке).
— Стимулирует рост патологических сосудов (неоваскуляризацию) — ключевой механизм при влажной форме ВМД и диабетической ретинопатии.
— Вызывает резистентность к инсулину (что ухудшает диабет).
Что показывает наука о связи с глазом:
— У пациентов с диабетической ретинопатией уровень IL-6 в стекловидном теле глаза повышен в 10–50 раз по сравнению с контролем.
— У пациентов с возрастной макулярной дегенерацией уровень IL-6 в крови коррелирует с риском прогрессирования и перехода в «влажную» форму.
— У пациентов с глаукомой повышенный IL-6 обнаруживается в слезной жидкости и водянистой влаге.
Клинический маркер: IL-6 можно измерить в крови. Уровни выше 5–7 пг/мл (в зависимости от лаборатории) считаются повышенными и ассоциируются с системным воспалением.
TNF-α: главный разрушитель
Фактор некроза опухоли альфа (TNF-α) — это, пожалуй, самый мощный провоспалительный цитокин. Его название говорит само за себя: в высоких концентрациях он способен убивать клетки.
Что делает TNF-α в норме:
— Участвует в защите от внутриклеточных бактерий и вирусов.
— Регулирует апоптоз (программируемую гибель клеток).
Что делает TNF-α при хроническом повышении:
— Вызывает лихорадку и потерю веса (кахексию).
— Повреждает эндотелий сосудов, повышает их проницаемость.
— Запускает каскад апоптоза в нейронах, включая ганглиозные клетки сетчатки.
— Участвует в формировании инсулинорезистентности.
Что показывает наука о связи с глазом:
— У пациентов с увеитом уровень TNF-α в водянистой влаге коррелирует с тяжестью воспаления.
— При глаукоме TNF-α напрямую убивает ганглиозные клетки сетчатки — это один из механизмов гибели нейронов при повышенном внутриглазном давлении.
— При диабетической ретинопатии TNF-α усиливает апоптоз перицитов — клеток, которые поддерживают капилляры сетчатки. Без перицитов сосуды становятся ломкими и образуют микроаневризмы.
Терапевтическая мишень: TNF-α настолько важен в патогенезе воспалительных заболеваний, что для его блокировки созданы специальные препараты — ингибиторы TNF (например, адалимумаб, инфликсимаб). Они успешно применяются при ревматоидном артрите, болезни Крона и — что важно для нас — при хронических увеитах, резистентных к стандартной терапии.
Но у этих препаратов есть побочные эффекты (риск инфекций). Поэтому гораздо разумнее — снижать уровень TNF-α за счёт уменьшения системного воспаления через кишечник.
IL-17: дирижёр аутоиммунного воспаления
Интерлейкин-17 (IL-17) — относительно недавно открытый цитокин (1993 год), но его роль оказалась огромной. IL-17 вырабатывается особым типом Т-лимфоцитов — Th17. А Th17-клетки, в свою очередь, активируются в кишечнике при определённых типах дисбиоза.
Что делает IL-17 в норме:
— Защита от грибковых и бактериальных инфекций (особенно на слизистых).
Что делает IL-17 при хроническом повышении:
— Привлекает нейтрофилы в ткани, вызывая гнойное воспаление.
— Участвует в аутоиммунных заболеваниях: псориаз, болезнь Крона, рассеянный склероз, ревматоидный артрит.
— Повреждает гемато-ретинальный барьер.
Что показывает наука о связи с глазом:
— IL-17 — ключевой цитокин при аутоиммунных увеитах. У пациентов с активным увеитом уровень IL-17 в крови и в водянистой влаге резко повышен.
— При синдроме сухого глаза IL-17 повреждает слёзные железы и вызывает апоптоз их клеток.
— При возрастной макулярной дегенерации IL-17 участвует в активации микроглии и хроническом воспалении сетчатки.
Связь с кишечником: Th17-клетки, вырабатывающие IL-17, в норме живут в кишечнике. Они помогают защищать слизистую от патогенов. Но при дисбиозе (особенно при росте Segmented Filamentous Bacteria у мышей, а у людей — некоторых видов Bacteroides и E. coli) эти клетки активируются чрезмерно, покидают кишечник и мигрируют в другие органы, включая глаз.
Это ещё один пример антигенной мимикрии (о которой мы подробнее поговорим в главе 4): белки некоторых кишечных бактерий похожи на белки сетчатки, и Th17-клетки по ошибке атакуют собственный глаз.
Три цитокина: сводная таблица
Бесплатный фрагмент закончился.
Купите книгу, чтобы продолжить чтение.